ДИСФУНКЦИЯ ЭНДОТЕЛИЯ И СИСТЕМА ГЕМОСТАЗА В ГРУППАХ РИСКА ПО РАЗВИТИЮ АКУШЕРСКОЙ ПАТОЛОГИИ. СИСТЕМНЫЙ ПОДХОД К ДИАГНОСТИКЕ И ТЕРАПИИ
Джобава Э.М., Некрасова К.Р., Артизанова Д.П., Хейдар Л.А., Судакова Г.Ю., Данелян С.Ж., Блинов Д.В., Доброхотова Ю.Э. Дата публикации на сайте: 2013-09-29 Доступна только on-line Резюме | Полный текст | Скачать в PDF
Резюме:
В данной статье описаны особенности системы гемостаза и функции эндотелия у беременных пациенток, относящихся к группе риска по развитию акушерских осложнений: хроническая артериальная гипертензия, сахарный диабет 1-го типа, гестационный сахарный диабет, эпилепсия, патология вен нижних конечностей, невынашивание беременности. На основании проведенного исследования разработан алгоритм диагностики дисфункции эндотелия и патологии системы гемостаза у данных пациенток. С учетом основных патогенетических аспектов приведена подробная фармакотерапия выявленной патологии. Разработана шкала «Оценки степени тромбофилии и методов её коррекции во время беременности и на фоне экстрагенитальной патологии®», которая позволяет определить и подобрать дифференцированную фармакотерапию с определенной дозировкой, длительностью курса и контролем в динамике, независимо от методов и норм определения параметров гемостаза.
ENDOTHELIAL DYSFUNCTION AND HEMOSTASIS SYSTEM IN PATIENTS AT RISK FOR OBSTETRIC PATHOLOGY. SYSTEMIC APPROACH TO DIAGNOSIS AND THERAPY
Jobava E.M. , Nekrasova К.R. , Artisanova D.P. , Heidar L.А. , Sudakova G.Yu. , Danelyan S.G. , Blinov D.V. , Dobrokhotova Yu.E.
GBOU VPO RNIMU named after N.I. Pirogov of Ministry of Healthcare of Russia, Moscow
GBUZ Maternity home №18 of Moscow Department of Healthcare
GBUZ Maternity home №5 of Moscow Department of Healthcare
Abstract: this article describes the features of the hemostatic system and endothelial function in pregnant patients who are at risk for obstetric complications: chronic hypertension, type 1 diabetes, gestational diabetes mellitus, epilepsy, a pathology of leg veins, miscarriage. Based on this study developed an algorithm for diagnosis of endothelial dysfunction and pathology of the hemostatic system in these patients. Given the major pathogenetic aspects, provides detailed pharmacotherapy revealed pathology. Developed a scale of «the assessment of the thrombophilia and methods of its correction during pregnancy and on the background of extragenital pathology®», which allows you to identify and find a differentiated pharmacotherapy with certain dosage, duration of the course in the dynamics and control, regardless of the methods and standards of determining the parameters of hemostasis.
Key words: pregnancy, endothelial dysfunction, hemostatic pathology, pharmacotherapy.
Ключевые слова: Беременность, дисфункция эндотелия, патология системы гемостаза, фармакотерапия.
Актуальность проблемы. В последние годы, в связи с ростом возраста первых родов и снижением общего состояния здоровья населения России, отмечается общий рост экстрагенитальной патологии среди беременных женщин и неуклонный рост акушерских осложнений. Одними из наиболее частых экстрагенитальных заболеваний во время беременности являются хроническая артериальная гипертензия (ХАГ), прегестационный (СД 1-го и 2-го типов) и гестационный сахарный диабет (ГСД), варикозная болезнь (ВБ), тромботические осложнения (тромбофлебит (ТФ), тромбоз глубоких вен (ТГВ)) и эпилепсия [1,2]. По данным современной литературы, наиболее приоритетной теорией общности патогенеза акушерских осложнений (в т.ч. на фоне экстрагенитальной патологии) является теория дисфункции эндотелия (ДЭ) и развивающихся на ее фоне нарушений в системе гемостаза [3]. Самый большой интерес в контексте ДЭ и тромбофилии представляют данные о влиянии различных лекарственных препаратов на функциональные характеристики эндотелия и возможность применения этих препаратов в акушерской практике. При огромном клиническом опыте, накопленном в области патогенетического (с точки зрения ДЭ и патологии системы гемостаза) лечения акушерских осложнений и экстрагенитальных заболеваний во время беременности, существуют определенные серьезные проблемы при выборе препарата для терапии [4]. Наряду с этим тенденцией современного акушерства в настоящее время является минимизация фармакотерапии. Основные разноречия существуют в значимости и нормах различных параметров системы гемостаза, в препаратах, курсах и дозировках, влияющих на эти параметры, а также в клинических показаниях. Изучению именно этой проблемы и созданию алгоритма терапии и посвящено данное исследование.
Цель работы: улучшить течение беременности и исходы родов в группах высокого риска по развитию акушерской патологии путем изучения особенностей системы гемостаза и функции эндотелия, а также систематизации подхода к диагностике и терапии выявленных нарушений.
Материалы и методы исследования
В целом в рамках исследования, проводившегося с 2003 по 2011 г., было обследовано 610 беременных, из которых 185 – вошли в исследование по ХАГ, 115 – в исследование по СД 1-го типа, 90 – в исследование по ГСД, 60 – в исследование по эпилепсии, 150 – в исследование по заболеваниям вен. Контрольную группу составили 70 беременных с физиологическим течением гестационного периода. Работа проводилась совместно с кафедрой неврологии и нейрохирургии ГБОУ ВПО РНИМУ, кафедрой эндокринологии и диабетологии ФУВ ГБОУ ВПО РНИМУ, кафедрой хирургических болезней ГБОУ ВПО РНИМУ. Также работа была выполнена совместно с лабораторией клинической иммунологии ФГБУ НЦАГ и П РАМН им. В.И. Кулакова Росмедтехнологий Минздрава России и лабораторией клеточной иммунопатологии и биотехнологии НИИ морфологии человека РАМН. В исследование по ХАГ было включено 185 беременных, которые были разделены на следующие группы: I группа (ХАГ) – 60 беременных с 22 недель гестации с ХАГ. II группа (ХАГ+ПЭ) – 60 беременных с 22 недель гестации, у которых ХАГ сопровождалась развитием ПЭ умеренной степени (гестоз средней степени тяжести). Группа сравнения (III группа) (ПЭ) – 65 пациенток с ПЭ умеренной степени (гестоз средней степени тяжести) с 22 недель гестации. В рамках исследования беременных с СД 1-го типа было обследовано 115 пациенток со сроком гестации от 22 недель и до родоразрешения. В I группу (основная) вошли 90 беременных с СД 1-го типа средней степени тяжести в стадии компенсации, осложненным умеренной ПЭ (гестоз средней степени тяжести) на фоне СД 1-го типа. II группу (сравнения) составили 25 беременных с умеренной ПЭ (гестоз средней степени тяжести) без СД 1-го типа, получавших традиционную терапию ПЭ (гестоза). В исследование по ГСД было включено 90 беременных, которые были разделены на следующие три группы. В I группу вошли 50 беременных с неинсулинопотребным ГСД в сроке гестации от 12 недель и до родоразрешения. II группу составили 40 беременных с инсулинопотребным ГСД в сроке гестации от 12 недель и до родоразрешения. В ходе выполнения поставленных задач в рамках исследования беременных с эпилепсией нами было обследовано 60 пациенток с эпилепсией, существовавшей до беременности в сроке беременности от 12 недель и до родоразрешения. Все обследованные пациентки были разделены по варианту противоэпилептической терапии (ПЭП) на a и b подгруппы. Также все пациентки были разделены на две группы по 30человек. В 1-й группе, помимо ПЭП и традиционного лечения развившихся акушерских осложнений, при выявлении ГГЦ дополнительно назначалась высокая доза фолиевой кислоты (ФК) (5 мг в сут.). Также в рамках проводимого исследования было обследовано 150 беременных с различными тромботическими осложнениями, поступивших в родильное и хирургическое отделение Московской городской клинической больницы №1 им. Н.И. Пирогова. Было сформировано несколько групп пациенток: 2-я группа – 60 беременных с варикозной болезнью (ВБ). 3-я группа – 30 пациенток с ВБ и тромбозом в анамнезе, включая и тех, у кого тромбоз был выявлен до включения в исследование во время настоящей беременности. 4-я группа – 30 беременных с ВБ и острым тромботическим процессом на момент исследования – тромбофлебит (ТФ). 5-я группа – 30 пациенток без ВБ и острым тромбозом в системе глубоких вен (ТГВ) во время настоящей беременности на момент исследования. По возрасту, основным особенностям анамнеза, характеру репродуктивной функции, наследственности беременные всех групп в каждом блоке исследования были в целом сопоставимы между собой.
При проведении исследования в программе обследования использовались традиционные для каждой экстрагенитальной патологии методы исследования. Исследование системы гемостаза и концентрации гомоцистеина проводилось на базе лаборатории клинической иммунологии ФГБУ НЦАГ и П РАМН традиционными методами. Определение метаболитов оксида азота (NOх) проводили флюориметрическим методом, определение уровня фибронектина (ФН) – при помощи метода твердофазового иммуноферментного анализа (ИФА), исследование на тромбофилические мутации – методом аллель-специфической ПЦР.
При выявлении тромбофилических нарушений гемостаза и ДЭ в терапию включались: при гиперагрегации или/и изолированном повышении маркеров тромбинемии – ацетилсалициловая кислота 125 мг в сут., при изолированной гиперагрегации – дипиридамол по 75 мг в сут. в течение трех недель или пентоксифиллин 300 мг в сут. При гиперкоагуляции назначались прямые антикоагулянты – сулодексид в дозе 600-1200 ЛЕ в сут. в/в, в/м или перорально, низкомолекулярные гепарины (НМГ) – надропарин в дозе от 0,3 мл (2850 МЕ) до 0,8 мл (7600 МЕ) или эноксапарин от 0,2 мл (2000 МЕ) до 0,8 мл (8000 МЕ) подкожно 1 или 2 раза в сут. в течение 10-14 дней. Также назначались препараты с умеренной активностью в отношении тромбофилических нарушений и разрешенные при беременности – диосмин 600 мг 2 раза в сут., эсцин 100-150 мг в сут., Магне В6 Форте (цитрат магния с пиридоксином) 1 таблетка 3 раза в сутки. В случае обнаружения ГГЦ в комплекс лечебных мероприятий включались ФК в высокой дозе (5 мг в сут.). Терапия подбиралась индивидуально с учетом показателей гемостаза, паритета, общего и репродуктивного анамнеза, сопутствующей патологии, срока беременности, акушерских осложнений и др. Также при развитии акушерских осложнений назначалась традиционная терапия, а в зависимости от экстрагенитальной патологии проводилась традиционная комплексная специфическая терапия: антигипертензивная, противоэпилептическая, инсулинотерапия, местная противовоспалительная и флебодинамическая.
Результаты и их обсуждение
У беременных с ХАГ развивается эндотелиальная дисфункция, достоверно более выраженная при присоединении гестоза (ПЭ) (см. табл. 1). Повышение метаболитов NO свидетельствует о напряжении компенсаторных реакций эндотелия. При их «истощении» формируется дефицит оксида азота. ГЦ и ФН имеют однонаправленные изменения, выражающиеся в достоверном повышении их концентрации, достоверно более выраженные при ХАГ, осложненной ПЭ (гестозом).
Таблица 1. Динамика изменения маркеров ДЭ на фоне лечения у беременных с ХАГ:
*р<0,05 при сравнении с данными в группе контроля;
**р<0,05 при сравнении с данными во ХАГ II и ХАГ III группах;
#р<0,05 при сравнении с данными в ХАГ III группе;
##р<0,05 при сравнении с данными в ХАГ I и ХАГ III группах.
| Маркеры дисфункции эндотелия | Группы обследованных (n=215) |
|---|
| ХАГ I (n=60) | ХАГ II (n=60) ХАГ+ПЭ | ХАГ III (n=65) ПЭ | Контроль (n=30) |
|---|
| NOx, ммоль/л | 12,4±0,2* | 5,3±0,21*# | 6,02±0,27* | 8,18±0,72 | | ГЦ, мкмоль/л | 9,1±0,4* | 11,7±0,27*## | 9,7±0,3* | 4,2±0,9 | | Фибронектин, мг/л | 849±13*# | 866±11*# | 793±11* | 485±18 |
Частота тромбофилических мутаций представлена на рисунке 1. Из рисунка видно, что мутация МТГФР, являясь генетической причиной ГГЦ и провоцируя ДЭ, может быть ассоциирована (или являться фактором риска) с развитием эссенциальной ХАГ, природа которой до сих пор до конца не ясна. В гемостазиограммах имела место активация факторов протромбинового комплекса, возрастание ИТП, повышение индуцированной агрегации тромбоцитов и рост маркеров хронической тромбинемии. У беременных ХАГ II группы по большинству показателей наблюдались достоверные различия по сравнению с пациентками ХАГ I и ХАГ III групп, что свидетельствует о более глубоком нарушении гемостаза тромбофилического характера у пациенток с ПЭ на фоне ХАГ (p<0,05).
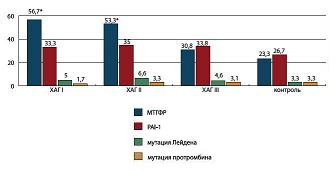 | Рисунок 1: Частота тромбофилических мутаций у беременных с ХАГ:
*р<0,05 при сравнении с данными в группе контроля. |
Распределение пациенток с ХАГ по принципу терапии представлено в таблице 2. При рандомизации на А и Б подгруппы использовался коэффициент, равный 0,5; т.е. распределение происходило 1:1 начиная с НМГ. При анализе маркеров ДЭ было выявлено достоверное снижение ГЦ во всех подгруппах и метаболитов NO в Б подгруппах (сулодексид) трех основных групп по сравнению с данными до лечения (p<0,05) (см. рис. 2).
Таблица 2. Распределение пациенток с ХАГ по подгруппам в зависимости от антикоагулянтной/дезагрегантной терапии (абсолютные числа).
| Препараты | ХАГ I (n=60) | ХАГ II (n=60) | ХАГ III (n=60) |
|---|
| Антикоагулянты: | 26 (43,3%) | 32 (53,3%) | 28 (43,1%) | | Надропарин (А подгруппа) | 13 | 16 | 14 | | Сулодексид (Б подгруппа) | 13 | 16 | 14 | | Дезагреганты: (В подгруппа) | 34 (56,7%) | 28 (46,7%) | 37 (56,9%) | | Дипиридамол | 8 | 6 | 9 | | Ацетилсалициловая кислота | 9 | 7 | 10 | | Пентоксифиллин | 8 | 8 | 9 | | Цитрат магния (+пиридоксин) | 9 | 7 | 11 |
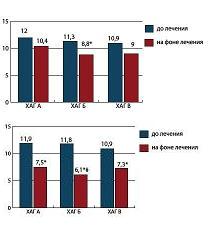 | Рисунок 2: Динамика концентрации метаболитов NO (ммоль/л) и ГЦ (мкмоль/л) у беременных ХАГ I группы на фоне лечения:
*р<0,05 при сравнении с данными в подгруппах до лечения;
#р<0,05 при сравнении с данными в А и В подгруппах после лечения. |
При этом в целом по динамике маркеров ДЭ меньшую чувствительность к терапии показала ХАГ II группа (ХАГ+ПЭ). Анализ параметров гемостаза выявил, что клинически значимое и достоверное улучшение определялось у всех пациенток без достоверных различий по подгруппам, что говорит о равной антикоагулянтной активности Клексана (эноксапарина) и Вессел Дуэ Ф (сулодексида) в отношении тромбофилических нарушений гемостаза.
При оценке функции фетоплацентарного комплекса в процессе проведения исследования (с 22 недель и до родоразрешения) в подгруппах ХАГ Б отмечалось достоверное снижение частоты развития ПН (в 2 раза), по сравнению с ХАГ А и В на 3,1% и 3,4% (p<0,05). Суммарная частота развития ПН была невелика и в ХАГ I группе составила 11,6% (7), в ХАГ II группе – 15% (9), в ХАГ III – 9,2% (6) случаев. При этом частота декомпенсации уже имеющейся ПН снизилась на 6,7%, а частота формирования СЗРП на фоне применения Вессел Дуэ Ф (сулодексида) в составе комплексной терапии – на 7,8%. Также отмечалось снижение частоты развития и прогрессирования ПЭ (гестоза) на 6,6% на фоне применения сулодексида в составе комплексной терапии. Интересным явилось достоверное снижение частоты преждевременных родов (ПР) на 3,1-5% у беременных, получавших антикоагулянтную терапию Вессел Дуэ Ф (сулодексидом) в составе комплексного лечения, по сравнению с терапией Клексаном (эноксапарином) и дезагрегантами. Анализ перинатальных исходов родов показал, что в ХАГ Б подгруппах в состоянии средней тяжести родилось 2 детей (11,8% при n=17), тогда как в ХАГ А подгруппах – 7 (41,2% при n=17) новорожденных, а в ХАГ В подгруппах – 8 (47% при n=17) (p<0,05). На основании этого можно сказать, что происходило снижение частоты неудовлетворительного состояния новорожденных на 7%.
У беременных с гестозом (ПЭ) и СД 1-го типа повреждение эндотелия происходит на более глубоком и выраженном уровне, чем при гестозе без СД 1-го типа (см. рис. 3). В целом те или иные проявления ДЭ были выявлены у всех беременных СД I и II групп, при этом изолированного изменения одного из маркеров ДЭ не обнаружено ни в одном случае. Анализ гемостазиограмм беременных СД I и II групп выявил, что в 100% наблюдений имели место какие-либо нарушения гемостаза. У 60 (66,7%) беременных с СД 1-го типа это потребовало проведения антикоагулянтной терапии (НМГ, сулодексид), в остальных 30 (33,3%) случаях – дезагрегантной терапии. По принципу терапии беременные с СД 1-го типа были разделены на три подгруппы: СД Iа, Iб и Iв. При рандомизации на СД Iа и СД Iб подгруппы использовался коэффициент, равный 0,49; т.е. распределение происходило 1:1 начиная с НМГ, но первая и последняя пары 1:2. В итоге СД Ia подгруппу составили 28 пациенток, которым назначался Фраксипарин (надропарин), СД Iб подгруппу – 32 пациентки, получавшие Вессел Дуэ Ф (сулодексид). В СД Iв подгруппу вошли 30 пациенток, не нуждавшихся в антикоагулянтной терапии, которым проводилась дезагрегантная терапия. Наиболее показательная динамика маркеров ДЭ представлена на рисунке 4.
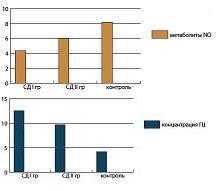 | Рисунок 3: Параметры метаболитов NO (ммоль/л) и ГЦ (мкмоль/л) в группах исследования беременных с СД 1-го типа:
*р<0,05 (различия статистически достоверны по отношению к контролю);
#р<0,05 (различия статистически достоверны по отношению к СД II группе). |
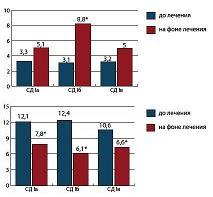 | Рисунок 4: Динамика концентрации метаболитов NO (ммоль/л) и ГЦ (мкмоль/л) у беременных с СД 1-го типа в зависимости от вида терапии:
*р<0,05 при сравнении с данными в подгруппах до лечения. |
При сравнительном анализе гемостазиограмм во всех подгруппах исследования до и через 14 дней после начала терапии отмечено существенное улучшение всех параметров гемостаза, но достоверные различия выявлены в СД Iа и СД Iб подгруппах по значениям ИТП, АВР, АЧТВ, ПТИ и концентрации фибриногена по сравнению с показателями до ле чения.
При оценке клинических показателей достоверные данные, свидетельствующие о нефропротекторном воздействии Вессел Дуэ Ф (сулодексида) при СД 1-готипа, были получены по динамике протеинурии. Интересно также, что при использовании Вессел Дуэ Ф (сулодексида) в составе комплексной терапии у 42% пациенток СД Iб подгруппы отмечалось снижение потребности в антигипертензивной терапии. При оценке состояния функциональной системы «мать-плацента-плод» на фоне дифференцированной терапии отмечено клинически значимое снижение значения СДО в сосудах фето-плацентарного комплекса.
При анализе динамики ДФ через 14 дней начала лечения нами установлено уменьшение степени ДФ, более выраженное в СД Iб подгруппе по сравнению с СД Iа, что, безусловно, подтверждает связь патогенетического звена ДФ с ДЭ и положительное влияние сулодексида непосредственно на эндотелий (см. табл. 3).
Таблица 3. Динамика ДФ на фоне лечения через 14 дней терапии у беременных с СД 1-го типа.
| Диабетическая фетопатия | Подгруппы обследованных (n=90) |
|---|
| СД Iа ( n=28) | СД iб ( n=32) | СД Iв ( n=30) |
|---|
| До лечения | На фоне лечения | До лечения | На фоне лечения | До лечения | На фоне лечения |
|---|
| ДФ нет | 11
(39,3%) | 15
(53,6%) | 12
(37,5%) | 18
(56,2%) | 11
(36,7%) | 13
(43,3%) | | Умеренная ДФ | 16
(57,1%) | 13
(46,4%) | 18
(56,3%) | 14
(43,8%) | 18
(60%) | 17
(56,7%) | | Выраженная ДФ | 1
(3,6%) | - | 2
(6,25%) | - | 1
(3,3%) | - |
Несмотря на полученный клинический эффект, подтвержденный общепринятыми лабораторными и специальными методами исследования, в рассматриваемой группе беременных с СД 1-го типа наблюдался высокий процент родоразрешений путем операции кесарева сечения – 69 (76,7%), что объясняется высокой степенью тяжести соматической патологии и выраженностью ДФ. При этом отмечалась недостоверная тенденция к улучшению исходов родов у беременных, получавших комплексную терапию с включением Вессел Дуэ Ф (сулодексида).
У беременных с инсулинопотребным ГСД повреждение эндотелия происходит на более глубоком уровне, чем у пациенток с неинсулинопотребной формой ГСД, но, в целом, ДЭ при ГСД носит менее выраженный характер, чем при СД 1-го типа. Изолированные изменения одного из маркеров ДЭ, такого как NO, были обнаружены в 16 и 10% случаев у беременных ГСД I и ГСД II групп соответственно. Анализ гемостазиограмм беременных с ГСД I и II групп выявил, что в большинстве наблюдений имели место какие-либо нарушения гемостаза: гиперкоагуляция, гиперагрегация, хроническая тромбинемия или их сочетания. При этом 20 (40%) беременных с неинсулинопотребным ГСД не нуждались в антикоагулянтной или/и дезагрегантной терапии. В дезагрегантной терапии нуждались 30 (42,9%) женщин (подгруппа В), из них 12 (40%) беременных ГСД II группы (инсулинопотребный ГСД) и 18 (60%) пациенток ГСД I группы (неинсулинопотребный ГСД). В терапии антикоагулянтами нуждались всего 40 (57,1%) беременных, из них 28 (70%) входили в ГСД II, а 12 (30%) – в ГСД I. В качестве антикоагулянтов применялись Фраксипарин (надропарин) (подгруппа А, n=20) и Вессел Дуэ Ф (сулодексид) (подгруппа Б, n=20), при рандомизации использовался коэффициент, равный 0,5, т.е. распределение проводилось 1:1 начиная с НМГ. Динамика маркеров ДЭ представлена в таблице 4.
Таблица 4. Динамика изменения маркеров ДЭ на фоне лечения у беременных с ГСД:
*р<0,05 при сравнении с данными в подгруппах до лечения.
| Маркеры дисфункции эндотелия | Подгруппы обследованных (n=70) |
|---|
| ГСД а подгруппа (n=20) | ГСД б подгруппа (n=20) | ГСД в подгруппа (n=30) |
|---|
| До лечения | На фоне лечения | До лечения | На фоне лечения | До лечения | На фоне лечения |
|---|
| NOx, ммоль/л | 6,1±0,6 | 8,0±0,8 | 6,2±0,4 | 9,1±0,2* | 6,9±0,2 | 7,4±0,5 | | ГЦ, мкмоль/л | 9,1±0,3 | 6,6±0,2* | 8,9±0,2 | 6,2±0,3* | 8,2±0,2 | 6,3±0,4* | | Фибронектин, мг/л | 649±11 | 546±12* | 657±10 | 528±11* | 548±12 | 521±13 |
При оценке состояния функциональной системы «мать-плацента-плод» на фоне дифференцированной терапии отмечены достоверные и клинически значимые изменения, более выраженные в Б подгруппе. При анализе динамики ДФ через 14 дней после начала лечения нами установлено уменьшение степени ДФ, достоверно более выраженное в ГСД Б подгруппе по сравнению с ГСД А. Частота развития гестоза (ПЭ) в ГСД А подгруппе (надропарин) была достоверно выше (12 (60%) пациенток) по сравнению с ГСД Б подгруппой беременных, принимавших сулодексид (7 (35%) пациенток) (p<0,05). По частоте развития ПН были получены аналогичные данные: в ГСД А подгруппе ПН развилась у 10 (50%) беременных, тогда как в ГСД Б – лишь у 6 (30%) (p<0,05). В подгруппе В ПН развилась у 8 (26,7%) пациенток. Интересным фактом, на наш взгляд, явилось то, что у пациенток с инсулинопотребным ГСД, получавшим антикоагулянтную терапию сулодексидом, отмечалось достоверное снижение потребности в инсулинотерапии. Из 14 беременных с инсулинопотребным ГСД (из подгруппы Б) терапия Вессел Дуэ Ф (сулодексидом) позволила в 5 (35,7%) случаях отказаться от применения инсулина, у 4 (28,6%) беременных отмечалось снижение суммарной дозы инсулина в 2 раза, у остальных беременных (5 (35,7%)) стало возможным снизить дозу короткого инсулина. Подобных закономерностей в подгруппах ГСД А и В выявлено не было. Ни в одном случае у пациенток из подгруппы ГСД Б в течение беременности не возникло показаний к назначению инсулино-терапии, тогда как в ГСД А и В подгруппах у 2 (10%) и 3 (10%) беременных в III триместре потребовалось проведение инсулинотерапии по показаниям со стороны плода (выраженность ДФ).
У беременных с эпилепсией (ЭП), независимо от варианта ПЭП (моно- или политерапия), по сравнению с группой контроля имело место достоверное повышение ГЦ и метаболитов NO (см. табл. 5).
Таблица 5. Маркеры ДЭ в группах исследования у беременных с эпилепсией:
*р<0,05 (различия статистически достоверны по отношению к контролю).
| Изучаемые показатели | Группы обследованных (n=80) |
|---|
| ЭП I группа (n=30) | ЭП II группа (n=30) | Контроль (n=20) |
|---|
| Уровень NOх ммоль/л | 12,2±0,3* | 12,4±0,2* | 9,2±0,4 | | Уровень ГЦ, мкмоль/л | 12,6±0,2* | 11,9±0,1* | 4,5±0,3 | | Уровень ФН, мг/л | 547±12 | 541±11 | 515±12 |
По ГЦ и NO были выявлены достоверно более выраженные изменения в подгруппах беременных, получавших политерапию ПЭП (ЭП b подгруппы) по сравнению с монотерапией (ЭП a подгруппы). Анализ гемостазиограмм беременных ЭП I и II групп выявил, что в большинстве наблюдений (93,3% (56) при n=60) выявлялось состояние изокоагуляции, присущее сроку беременности и сравнимое с группой контроля. Нарушения гемостаза у беременных с эпилепсией проявлялись в активации тромбоцитарного звена, как первого и более раннего этапа активации системы гемостаза. Лишь у 4 (6,7%) беременных с эпилепсией (по две пациентки в ЭП I и II группах соответственно) была выявлена необходимость в антикоагулянтной терапии (Вессел Дуэ Ф (сулодексид)). При этом в 68,3% (41) наблюдений (n=60) у беременных с эпилепсией присутствовала гиперагрегация, потребовавшая назначения дезагрегантной терапии (20 (66,7%) и 21 (70%) пациентка из ЭП I и II группы соответственно). Зависимости показателей гемостаза от состава ПЭП терапии (ЭП a и b подгруппы) и частоты приступов во время беременности мы не выявили.
По данным УЗИ, различные признаки ПН были выявлены у 21 (35%) беременных с эпилепсией, и ни в одном случае у пациенток группы контроля. При этом ПН в 100% случаев развивалась у пациенток с наличием приступов во время беременности. Обращало на себя внимание то, что частота развития ПН и СЗРП была выше у пациенток, получавших политерапию ПЭП (13 (61,9%) против 8 (38,1%) случаев на монотерапии ПЭП, при n=21; p<0,05). При оценке фетометрии наиболее интересные результаты были получены при сравнении беременных, имевших приступы во время беременности (n=30) и без них (n=30). У беременных с эпилепсией и приступами во время беременности отмечалось снижение темпов прироста параметров фетометрии и развитие гипотрофии плода. При анализе течения беременности и исходов родов обращало на себя внимание то, что у пациенток с приступами эпилепсии во время беременности частота ПЭ (гестоза) была достоверно выше (12 (40%)) по сравнению с пациентками, не имевшими приступов эпилепсии во время беременности (5 (16,7%)) (p<0,05). Зависимости частоты ПЭ от состава ПЭП терапии (моноили политерапия) мы не выявили. Также у пациенток с приступами эпилепсии во время беременности была в 3 раза выше частота ПР (6 (20%)) по сравнению с пациентками, не имевшими приступов эпилепсии во время беременности (2 (6,7%)) (p<0,05).
При сравнительном анализе ЭП I и II групп беременных (эпилепсия) было выявлено достоверное снижение концентрации ГЦ уже в первые 14 дней терапии при назначении комбинации высоких доз ФК (5 мг в сут.) с витаминами группы В в составе комплексной терапии (ЭП I группа) по сравнению с ЭП II группой (p<0,05). При этом были выявлены различия достоверного характера на фоне лечения по концентрации NO в подгруппах ЭП a и b в зависимости от моно- или политерапии ПЭП. При анализе параметров гемостаза через 14 дней после начала лечения по вышеуказанным схемам наблюдалось клинически значимое улучшение показателей в обеих группах. Но достоверные изменения по сравнению с исходными данными были выявлены только по индуцированной агрегации тромбоцитов на АДФ (см. рис. 5) (р<0,05). Однако максимальный темп снижения наблюдался у пациенток из ЭП Ia подгруппы (на монотерапии ПЭП и ФК 5 мг в сут.). Минимальный темп снижения агрегации был выявлен у беременных на политерапии ПЭП и ФК в дозе 800 мкг в сут. (IIb подгруппа).
 | Рисунок 5: Динамика агрегации тромбоцитов (индуцированной на АДФ в %) на фоне лечения в группах исследования беременных с эпилепсией:
*р<0,05 (различия статистически достоверны по сравнению с исходными данными. |
При анализе частоты акушерских осложнений в ЭП I группе ПЭ (гестоз) развилась лишь у 6 (20%) пациенток. Тогда как в ЭП II группе ПЭ (гестоз) была диагностирована практически в 2 раза чаще – у 11 (36,7%) беременных (p<0,05). Аналогичная картина наблюдалась по частоте ПН. Так, в ЭП I группе (5 мг ФК) ПН была выявлена у 7 (23,3%) беременных, тогда как в ЭП II группе (800 мкг ФК) данный показатель составил 14 (46,7%) (p<0,05). При этом подавляющее большинство случаев СЗРП относилось именно к ЭП II группе (13 случаев из 15 (86,7%)). Основные показатели состояния новорожденных представлены в таблице 6.
Таблица 6. Основные показатели состояния новорожденных:
*р<0,05 (различия статистически достоверны между пациентками ЭП I и II групп);
**р<0,05 (различия статистически достоверны между пациентками ЭП I и контроля);
#р<0,05 (различия статистически достоверны между пациентками ЭП II и контроля).
| Показатель | ЭП I (n=30) | ЭП II (n=30) | Контроль (n=20) |
|---|
Оценка по Апгар на 1 мин, баллы
Оценка по Апгар на 5 мин, баллы | 7,12±0,21
7,86±0,38 | 6,19±0,3*
6,96±0,22* | 8,27±0,35#**
8,99±0,24#** | | Средняя масса тела, г | 3501±71 | 3120±63* | 3701±12#** | | Массо-ростовой коэффициент (МРК), ед. | 63±1 | 61±1 | 64±2 | | Признаки синдрома задержки роста плода (СЗРП) | 2 (6,6%) | 13 (43,3%)* | 0 (0%) | | Признаки морфофункциональной незрелости | - | 3 (10,0%) | 0 (0%) | | Мекониальные околоплодные воды | 1 (3,3%) | 7 (23,3%)* | 0 (0%) | | Относительная короткость пуповины | 5 (16,7%) | 6 (20%) | 1(5%) | | Перевод в детскую клиническую больницу (ДКБ) | 1 (3,3%) | 2 (6,7%) | 0 (0%) |
Большая часть новорожденных из ЭП I группы (5 мг ФК) родились с весом в пределах 3000-3500 г и более, тогда как в ЭП II группе приблизительно равное количество новорожденных при рождении имели вес до 3000 и 3000-3500 г. Представленные результаты подтверждают связь ГГЦ с ДЭ и роль ДЭ в генезе акушерских осложнений у беременных с эпилепсией, а также свидетельствуют о положительном влиянии комплексной дифференцированной терапии с включением высоких доз ФК на ГГЦ, ДЭ и патологию системы гемостаза, а следовательно, на функционирование ФПК и на перинатальные исходы при беременности, осложненной эпилепсией.
У беременных с заболеваниями вен нижних конечностей была выявлена высокая частота генетических форм тромбофилии. При анализе мультифакториальных форм генетической тромбофилии обращало на себя внимание, что во всех случаях выявления мутации в гене PAI-1 имелась и мутация в гене МТГФР. При определении уровня ФН сыворотки крови были выявлены изменения концентрации, характеризующие определенную степень остроты тромботического процесса (см. рис. 6).
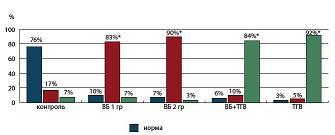 | Рисунок 6: Показатели ФН в группах исследования у беременных с патологией вен нижних конечностей:
*р<0,05 (различия достоверны по сравнению с контролем). |
Выявленные изменения концентрации ФН соответствовали активности процесса тромбообразования (по данным литературы), т.е. повышение уровня ФН наблюдалось при хронической тромбинемии (хроническом ДВС-синдроме), а резкое снижение – при остром тромботическом процессе. При анализе концентрации метаболитов NO было выявлено их достоверное снижение в группах с ТФ или ТГВ в настоящую беременность или в анамнезе по сравнению с контрольной (9,8±0,3 ммоль/л). Концентрация метаболитов NO, в отличие от ГГЦ, не имела динамики по группам. Однако в ВБ 1-й группе (неосложненная ВБ) в 95% (57) наблюдений была выявлена обратно противоположная динамика NO, а точнее – повышение метаболитов NO более 10,0 ммоль/л. В среднем показатель в ВБ 1-й группе составил 12,4±0,3 ммоль/л, что достоверно отличалось при сравнении с пациентками других групп (p<0,05). При патологии вен и тромботических осложнениях у беременных ГГЦ можно рассматривать не столько как маркер ДЭ, а в большей степени как молекулярный фактор тромбофилии (причина и следствие), тогда как ФН, на наш взгляд, является значимым маркером ДЭ и молекулярным фактором тромбофилии в прогнозировании предтромботического состояния.
В процессе проведения исследования в первую очередь были сформированы ВБ 1 и ВБ 2 группы, и в них мы сочли возможным провести сравнительное исследование влияния дополнительного назначения в составе комплексной терапии комбинации ФК (5 мг в сут.) и Магне В6 Форте (цитрат магния+пиридоксин) на показатели ГЦ, NO, ФН и гемостаза. Рандомизация в подгруппы проводилась с коэффициентом, равным 0,5, т.е. 1:1, включение начиналось с комбинации ФК с цитратом магния. В последующем исследование было расширено до групп ВБ+ТГВ и ТГВ, и у этих пациенток, с учетом уже полученных результатов, сравнительных исследований из этических соображений не проводилось, т.е. при выявлении ГГЦ и ДЭ всем назначалась комбинированная терапия в составе комплексного лечения. Вся терапия во всех группах назначалась совместно с сосудистыми хирургами и была комплексной и строго индивидуализированной.
Наиболее интересна была динамика концентрации NO и ФН у беременных с ТГВ на фоне и без ВБ (см. рис. 7, 8). Исходя из полученных данных обнаружено, что влияние комбинации ФК и Магне В6 Форте (цитрат магния с пиридоксином) в составе комплексной терапии на концентрацию ГЦ и ФН наиболее выражено при остром тромботическом процессе и менее – при хроническом ДВС синдроме. Концентрация метаболитов NO при этом является менее быстрореагирующим и менее лабильным показателем. Однако применение комбинации в профилактических целях у беременных с угрозой тромботических осложнений не менее эффективно нормализует уровень ГЦ и значительно снижает риск развития тромбоза. По показателям гемостаза отмечалось клинически значимое улучшение, вплоть до полной нормализации, достоверные различия были получены по большинству показателей (p<0,05).
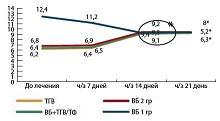 | Рисунок 7: Динамика изменения уровня метаболитов NO в процессе комплексной терапии у беременных с патологией вен нижних конечностей:
*р<0,05 (статистически достоверное изменение уровня NO на 14-й день лечения в сравнении с исходным значением). |
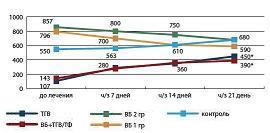 | Рисунок 8: Динамика изменения уровня ФН в процессе комплексного лечения с включением ФК у беременных с патологией вен нижних конечностей:
*р<0,05 – достоверное повышение ФН в сравнении с исходным уровнем. |
Интересным явилось то, что у 8 (13,3%) женщин, не получавших фолиевую кислоту и Магне В6 Форте в силу индивидуальной непереносимости, на 2-3-е сутки послеродового периода развился острый восходящий ТФ подкожных вен и у них была произведена операция Троянова-Тренделенбурга (перевязка сафено-феморального соустья) с назначением в последующем антикоагулянтной терапии. Также интересным фактом является то, что частота гестоза и ПН (кроме ВБ 1 группы) была сравнима с общепопуляционными показателями, хотя при тяжести данных осложнений мы ожидали большей частоты. Во всех клинических группах не было ни одного случая перинатальных потерь или тяжелых форм ПЭ (гестоза). На наш взгляд, это может быть связано с проведением комплексной терапии, включающей НМГ, дезагреганты, ФК и другие вышеуказанные препараты, которые в комбинации обладали стабилизирущим действием на эндотелий, и являлись, своего рода, профилактикой развития гестоза и ПН.
Выводы и рекомендации
У беременных из групп риска развивается ДЭ и тромбофилические изменения гемостаза, обуславливающие высокую частоту последующих акушерских осложнений. Беременным групп риска (ХАГ, СД 1-го типа, ГСД, эпилепсии, патология вен нижних конечностей, невынашивание беременности) по развитию акушерских осложнений рекомендуется исследовать систему гемостаза не реже 1 раза в месяц. При выборе препарата и курса антикоагулянтной или/и дезагрегантной терапии беременным с тромбофилическими нарушениями гемостаза, в том числе из групп риска по развитию акушерских осложнений, рекомендуется использовать разработанную нами шкалу «Оценки степени тромбофилии и методов ее коррекции во время беременности и на фоне экстрагенитальной патологии®», которая позволяет, исходя из суммы баллов, рассчитанных путем математического анализа на основании срока беременности, исходной экстрагенитальной патологии, общего и репродуктивного анамнеза, акушерских осложнений и результатов лабораторного обследования (маркеры ДЭ, генетические формы тромбофилии и параметры системы гемостаза), определить и подобрать дифференцированную фармакотерапию с определенной дозировкой, длительностью курса и контролем в динамике, независимо от методов и норм определения параметров гемостаза.
Литература:
1. Абрамченко В.В. Рациональная фармакотерапия патологии беременности и родов / В.В. Абрамченко, И.Н. Бойко. Спб. 2004; 304 с.
2. Сухих Г.Т., Вихляева Е.М., Ванько Л.В. и др. Эндотелиальная дисфункция в генезе перинатальной патологии. Акушерство и гинекология. 2008; 5: 3-7.
3. Omar Farouque H.M., Meredith I.T. Relative contribution of vasodilator prostanoids, NO, and KATP channels to human forearm metabolic vasodilation. Am. J. Physiol. Heart Circ. Physiol. 2003; 284: 2405-2411.
4. Szecsi P.B., Jorgensen M., Klajnbard A., Andersen M.R., Colov N.P., Stender S. Haemostatic reference intervals in pregnancy. Thromb Haemost. 2010 Apr.; 103 (4): 718-27. Epub. 2010. Feb. 19.
ENDOTHELIAL DYSFUNCTION AND HEMOSTASIS SYSTEM IN PATIENTS AT RISK FOR OBSTETRIC PATHOLOGY. SYSTEMIC APPROACH TO DIAGNOSIS AND THERAPY
Jobava E.M.1, Nekrasova К.R.1, Artisanova D.P.1, Heidar L.А.1, Sudakova G.Yu.3, Danelyan S.G.2, Blinov D.V.1, Dobrokhotova Yu.E.1
1 GBOU VPO RNIMU named after N.I. Pirogov of Ministry of Healthcare of Russia, Moscow
2 GBUZ Maternity home №18 of Moscow Department of Healthcare
3 GBUZ Maternity home №5 of Moscow Department of Healthcare
Abstract: this article describes the features of the hemostatic system and endothelial function in pregnant patients who are at risk for obstetric complications: chronic hypertension, type 1 diabetes, gestational diabetes mellitus, epilepsy, a pathology of leg veins, miscarriage. Based on this study developed an algorithm for diagnosis of endothelial dysfunction and pathology of the hemostatic system in these patients. Given the major pathogenetic aspects, provides detailed pharmacotherapy revealed pathology. Developed a scale of «the assessment of the thrombophilia and methods of its correction during pregnancy and on the background of extragenital pathology®», which allows you to identify and find a differentiated pharmacotherapy with certain dosage, duration of the course in the dynamics and control, regardless of the methods and standards of determining the parameters of hemostasis.
Key words: pregnancy, endothelial dysfunction, hemostatic pathology, pharmacotherapy. |
|